Abstract
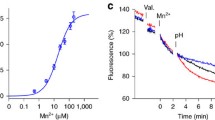
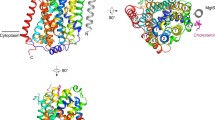
SLC23 family members transport either nucleobases or vitamin C. While the structure of SLC23 nucleobase transporters is resolved in high detail, their transport mechanism is not: they have been proposed, but not formally shown, to be proton-coupled symporters. Here, by establishing the first in vitro transport assay for this protein family, we demonstrate that a representative member of the SLC23 nucleobase transporters operates as a uniporter instead.
Article PDF
Similar content being viewed by others
Avoid common mistakes on your manuscript.
Literatur
Lu F, Li S, Jiang Y et al. (2011) Structure and mechanism of the uracil transporter UraA. Nature 472: 243–247
Alguel Y, Amillis S, Leung J et al. (2016) Structure of eukaryotic purine/H+ symporter UapA suggests a role for homodimerization in transport activity. Nat Commun 7: 11336
Botou M, Lazou P, Papakostas K et al (2018) Insight on specificity of uracil permeases of the NAT/NCS2 family from analysis of the transporter encoded in the pyrimidine utilization operon of Escherichia coli. Mol Microbiol 108: 204–219
Andersen PS, Frees D, Fast R, Mygind B (1995) Uracil uptake in Escherichia coli K-12: isolation of uraA mutants and cloning of the gene. J Bacteriol 177: 2008–2013
Wilks JC, Slonczewski JL (2007) pH of the cytoplasm and periplasm of Escherichia coli: rapid measurement by green fluorescent protein fluorimetry. J Bacteriol 189: 5601–5607
Holzhüter K, Geertsma ER (2022) Uniport, not proton-symport, in a non-mammalian SLC23 transporter. J Mol Biol, doi: https://doi.org/10.1016/j.jmb.2021.167393
Bagnara AS, Finch LR (1974) The effects of bases and nucleosides on the intracellular contents of nucleotides and 5-phosphoribosyl 1-pyrophosphate in Escherichia coli. Eur J Biochem 41: 421–430
Burton K (1977) Transport of adenine, hypoxanthine and uracil into Escherichia coli. Biochem J 186: 195–204
Funding
Open Access funding enabled and organized by Projekt DEAL.
Author information
Authors and Affiliations
Corresponding author
Additional information
Danksagung
Diese Arbeit wurde durch SFB807 und das CEF-MC unterstützt.
Katharina Holzhüter Jahrgang 1991. Biochemiestudium an der Universität Frankfurt a. M. Seit 2016 Promotion am Institut für Biochemie, Universität Frankfurt a. M.
Eric R. Geertsma Jahrgang 1976. Biochemiestudium an der Universität Groningen, Niederlande. 2005 Promotion. 2005–2008 Postdoc an der Universität Groningen. 2008–2013 Postdoc als FEBS- und HFSP-Fellow an der Universität Zürich, Schweiz. 2014–2020 Juniorprofessor am Institut für Biochemie, Universität Frankfurt a. M. Seit 2020 Technology Development Gruppenleiter am Max-Planck-Institut für molekulare Zellbiologie und Genetik, Dresden.
Rights and permissions
Dieser Artikel wird unter der Creative Commons Namensnennung 4.0 International Lizenz veröffentlicht, welche die Nutzung, Vervielfältigung, Bearbeitung, Verbreitung und Wiedergabe in jeglichem Medium und Format erlaubt, sofern Sie den/die ursprünglichen Autor(en) und die Quelle ordnungsgemäß nennen, einen Link zur Creative Commons Lizenz beifügen und angeben, ob Änderungen vorgenommen wurden. Die in diesem Artikel enthaltenen Bilder und sonstiges Drittmaterial unterliegen ebenfalls der genannten Creative Commons Lizenz, sofern sich aus der Abbildungslegende nichts anderes ergibt. Sofern das betreffende Material nicht unter der genannten Creative Commons Lizenz steht und die betreffende Handlung nicht nach gesetzlichen Vorschriften erlaubt ist, ist für die oben aufgeführten Weiterverwendungen des Materials die Einwilligung des jeweiligen Rechteinhabers einzuholen. Weitere Details zur Lizenz entnehmen Sie bitte der Lizenzinformation auf http://creativecommons.org/licenses/by/4.0/deed.de.
About this article
Cite this article
Holzhüter, K., Geertsma, E.R. SLC23-Nukleobasentransport entschlüsselt. Biospektrum 28, 27–29 (2022). https://doi.org/10.1007/s12268-022-1690-0
Published:
Issue Date:
DOI: https://doi.org/10.1007/s12268-022-1690-0